-
摘要:背景
糖尿病是重要的公共卫生问题之一,研究证明大气污染是糖尿病的危险因素之一。
目的评价大气污染物短期暴露对上海市静安区居民糖尿病相关疾病死亡的影响。
方法收集2013—2019年每日大气污染物数据、气象数据和居民糖尿病相关疾病死亡资料,采用时间序列分析方法的广义相加模型来评估大气污染物对居民糖尿病相关疾病死亡的短期效应;并根据不同性别、年龄进行分层分析,探索不同人群对大气污染物暴露的敏感性。
结果PM2.5、PM10、SO2、NO2质量浓度每增加10 μg·m−3,糖尿病相关疾病死亡风险在lag05分别增加2.47%(95%
CI : 1.56%~3.38%)、2.02%(95%CI : 1.29%~2.75%)、5.75%(95%CI : 2.99%~8.58%)和3.93%(95%CI : 2.49%~5.39%)(P <0.05)。PM2.5、PM10、SO2、NO2浓度升高会增加男性、女性和≥65岁人群糖尿病相关疾病死亡风险(P <0.05);但大气污染对糖尿病相关疾病死亡的影响在不同性别、年龄组间效应值的差异均无统计学意义。结论上海市静安区大气污染物PM2.5、PM10、SO2、NO2浓度升高会导致人群糖尿病相关疾病死亡风险增加,且存在滞后效应和累积效应,≥65岁人群是受大气污染对糖尿病相关疾病死亡影响的易感人群。
Abstract:BackgroundDiabetes mellitus is a major public health issue at present. Previous studies have shown that ambient air pollution is a risk factor for diabetes.
ObjectiveThis study aims to explore the acute effects of ambient air pollution on diabetes related death in Shanghai Jing’an District.
MethodsDaily air pollution data, meteorological data, and diabetes related mortality data in 2013−2019 in Shanghai Jing’an District were collected. A generalized additive model (GAM) was established to conduct time-series analysis on the short-term effect of ambient air pollution on diabetes related mortality, and gender- and age-stratified analysis on susceptibility of various groups to ambient air pollution exposures.
ResultsFor every 10 μg·m−3 increase of the concentrations of PM2.5, PM10, SO2, and NO2, the diabetes related mortality increased by 2.47% (95%
CI : 1.56%−3.38%), 2.02% (95%CI : 1.29%−2.75%), 5.75% (95%CI : 2.99%−8.58%), and 3.93% (95%CI : 2.49%−5.39%) at lag05 respectively (P <0.05). In the stratified analysis, exposures to increased concentrations of PM2.5, PM10, SO2, and NO2 raised the mortality risks from diabetes in male, female, and ≥65 years oldgroups (P <0.05). However, the differences in mortality risks from diabetes due to air pollution within gender and age groups were statistically insignificant.ConclusionIn Shanghai Jing'an District, the elevated levels of ambient air pollutants, including PM2.5, PM10, SO2, and NO2, are significantly associated with the increase of diabetes related mortality, and there are lag effects and cumulative effects. The ≥65 years olds are more susceptible to the impact of air pollution on diabetes related deaths.
-
Keywords:
- air pollution /
- diabetes /
- mortality /
- time-series analysis /
- generalized additive model
-
糖尿病作为主要慢性非传染性疾病之一,近年来死亡率和患病率持续上升[1-2],严重危害人群健康,是21世纪全球性的公共卫生挑战之一。根据《2019年上海市统计年鉴》[3],以糖尿病为主的内分泌营养代谢疾病是影响居民健康的第四位死亡疾病,是威胁居民健康的主要原因之一。传统的糖尿病危险因素包括肥胖、家族史、高血压、心脑血管疾病史、缺乏锻炼等[4]。近年来研究发现,大气污染与糖尿病也密切相关,是糖尿病的危险因素之一[5]。在2007—2017年的十年间,大气污染造成全球糖尿病死亡人数增加了50.7%,死亡率增加了11.1%[6]。国外一些研究发现大气污染物暴露会增加人群糖尿病死亡的风险[7-9],目前国内关于大气污染对糖尿病死亡影响的研究较少。研究发现暴露于大气污染会引起氧化应激和炎症[10-11]、内皮功能障碍[10]、自主神经系统失衡[12]、血糖升高[13-14]、胰岛素抵抗[15]等,进而影响糖尿病的进展,增加糖尿病发病和死亡风险,上述研究为大气污染与糖尿病死亡风险的关联提供了合理的生物学机制。由于糖尿病患者一般患有多种疾病,因此对于糖尿病根本死因的判定存在很大差异,使用死亡证明中的根本死因进行统计可能会低估50%的糖尿病死亡[16]。故研究人员通过研究糖尿病患者的死亡数据或者死亡证明中所有提及糖尿病死亡的数据即糖尿病相关疾病死亡数据,以全面评估糖尿病死亡状况[17-19]。本研究拟利用死亡数据、大气污染物数据及气象数据,采用时间序列分析方法,评价大气污染物短期暴露对上海市静安区居民糖尿病相关疾病死亡的影响,为制定相关的环保措施和保护易感人群提供依据。
1. 材料与方法
1.1 资料来源
2013年1月1日—2019年12月31日上海市静安区居民死亡数据来源于上海市静安区疾病预防控制中心死因登记系统。本研究死亡原因根据国际疾病分类第十版(International Classification of Disease-10, ICD-10)进行分类,糖尿病相关疾病死亡的数据采用死亡原因中所有提及糖尿病的非意外死亡数据(E10~E14)。同时期的大气污染物数据(PM2.5、PM10、SO2、NO2)来源于上海市静安区环境监测站(上海闵行区青悦环保信息技术服务中心提供,该中心业务主管单位为上海市闵行区环保局)。气象数据(气温和相对湿度)来源于中国气象数据网(http://data.cma.cn)。由于静安区无气象观测站,故本研究采用距离静安区最近观测站即宝山观测站(经度31°24’,纬度121°27’)的数据替代。本研究已获上海市静安区疾病预防控制中心伦理委员会批准(无编号)。
1.2 研究方法
使用时间序列分析法对大气污染与糖尿病相关疾病死亡的关联进行分析。居民每日糖尿病相关疾病死亡相对于总人口而言属于小概率事件,其分布近似于泊松分布。构建泊松回归的广义相加模型,采用自然样条平滑函数控制长期趋势、气象等混杂因素,分别评估PM2.5、PM10、SO2、NO2的浓度变化对居民糖尿病相关疾病死亡的影响。具体公式如下:
$$ log[E(Y_{t})]= α+ \beta Z_{t}+ ns(T, V_{df})+ ns(X_{t}, V_{df})+ V_{{\rm{DOW}}} $$ 其中t为观察日期,Yt为观察日期t时的糖尿病相关疾病死亡人数,E(Yt)为观察日期t时糖尿病相关疾病死亡的期望人数;α为截距;
$\beta $ 为回归系数;Zt为观察日期t当天大气污染物平均浓度;ns为自然样条平滑函数;T为时间序列,用于控制长期趋势与周期效应;Xt为可能产生影响的气温、相对湿度等混杂因素;VDOW为哑变量,用于控制星期几效应;Vdf为自由度,根据赤池信息准则,选择时间变量自由度为7·年−1,气温的自由度为7,相对湿度的自由度为4。由于大气污染物存在滞后性和累积性,故本研究对当日至前5日单日滞后(lag0~lag5)的污染物浓度和当日至前1~5 d(lag01~lag05)的污染物浓度移动平均值进行分析。选择单污染物模型中各污染物对糖尿病相关疾病死亡有统计学意义的最强效应滞后时间,进行双污染物模型拟合,评估主模型的稳健性;按照性别(男性和女性)、年龄(<65岁和≥65岁)进行分层分析,效应差别检验使用Z检验,公式如下:
$$ Z=(E_{1}-E_{2})/ \sqrt{\mathrm{S}\mathrm{E}{({E}_{1})}^{2}+\mathrm{S}\mathrm{E}{({E}_{2})}^{2}} $$ 式中,E1和E2为各层的效应值,SE(E1)和SE(E2)为标准误。
选择有统计学意义的最强效应滞后时间的大气污染物(PM2.5、PM10、SO2、NO2)浓度,分别绘制暴露-反应关系曲线。
1.3 统计学分析
采用R 3.5.3软件进行统计分析。运用描述性分析研究人群糖尿病相关疾病死亡、大气污染物和气象指标,运用Spearman秩相关分析大气污染物与气象指标之间的关系。大气污染物效应的评价指标采用超额危险度(excess risk, ER),即大气污染物质量浓度(简称浓度)每上升10 μg·m−3,居民糖尿病相关疾病死亡增加的百分比。检验水准α=0.05。
2. 结果
2.1 基本情况
2013年1月1日—2019年12月31日,上海市静安区糖尿病相关疾病死亡共10 904例,男性5 398例,女性5 506例,<65岁1 198例,≥65岁9 706例,日均死亡数分别为4.27、2.11、2.15、0.47、3.80例。大气污染物PM2.5、PM10、SO2、NO2日平均浓度分别为47.16、68.12、14.09、46.29 μg·m−3。根据GB 3095—2012《环境空气质量标准》,SO2和NO2达到国家环境空气质量一级标准(分别为50和80 μg·m−3),PM2.5和PM10达到国家环境空气质量二级标准(分别为75和150 μg·m−3)。气象指标日均温度和湿度分别为17.48℃和72.71%(表1)。
表 1 2013—2019年上海市静安区糖尿病相关疾病死亡、大气污染物浓度水平及气象因素的分布Table 1. Daily diabetes related deaths, concentrations of air pollutants, and levels of meteorological factors in Shanghai Jing'an District from 2013 to 2019指标 ${\bar x}$±s Min P25 P50 P75 Max 死亡指标 糖尿病相关疾病死亡人数 4.27±2.22 0.00 3.00 4.00 6.00 16.00 男性 2.11±1.50 0.00 1.00 2.00 3.00 11.00 女性 2.15±1.52 0.00 1.00 2.00 3.00 9.00 <65岁 0.47±0.69 0.00 0.00 0.00 1.00 4.00 ≥65岁 3.80±2.08 0.00 2.00 4.00 5.00 15.00 大气污染物浓度/(μg·m−3) PM10 68.12±42.60 7.00 40.20 57.17 82.54 561.32 PM2.5 47.16±34.23 4.67 23.63 38.38 59.55 505.78 SO2 14.09±10.96 1.74 7.50 11.04 16.84 105.70 NO2 46.29±21.67 5.08 30.57 42.17 57.64 157.63 气象指标 温度/℃ 17.48±8.72 −6.10 9.80 18.40 24.40 35.00 相对湿度/% 72.71±12.55 27.50 64.30 74.00 82.00 99.30 2.2 大气污染物与气象指标的相关性
PM10和PM2.5之间存在高度相关性,相关系数为0.88。此外SO2、NO2、PM10和PM2.5之间存在中等强度正相关,相关系数0.61~0.68。温度和相对湿度与大气污染物指标之间均呈负相关(表2)。
表 2 2013—2019年上海市静安区大气污染物与气象因素相关性分析(r)Table 2. Correlation analysis between air pollutants and meteorological factors in Shanghai Jing'an District from 2013 to 2019 (r)指标 PM2.5 SO2 NO2 温度 相对湿度 PM10 0.88* 0.62* 0.64* −0.22* −0.32* PM2.5 1.00 0.61* 0.68* −0.27* −0.13* SO2 1.00 0.61* −0.45* −0.41* NO2 1.00 −0.51* −0.10* 温度 1.00 0.12* [注] *:P< 0.05。 2.3 单污染物模型结果
大气污染物对人群糖尿病相关疾病死亡风险的单日滞后结果显示,PM2.5、PM10、NO2在lag0~lag5均有统计学意义(P<0.05),SO2在lag1~lag5有统计学意义(P<0.05)。PM2.5、PM10、SO2、NO2的单日滞后效应分别在lag4、lag3、lag3、lag1最大,其对应的ER及其95%CI分别为1.20%(0.64%~1.76%)、1.05%(0.61%~1.50%)、4.54% (2.51%~6.60%)和2.44%(1.45%~3.44%)(表3)。
表 3 2013—2019年上海市静安区大气污染物对糖尿病相关疾病死亡的超额危险度[ER(95%CI)/%]Table 3. Excess risk of diabetes related mortality in association with air pollutants in Shanghai Jing'an District from 2013 to 2019 [ER(95%CI)/%]滞后天数 PM2.5 PM10 SO2 NO2 lag0 0.78(0.22~1.35)* 0.63(0.17~1.10)* 0.89(−1.26~3.08) 1.04(0.06~2.04)* lag1 1.11(0.55~1.68)* 0.90(0.44~1.36)* 3.32(1.23~5.47)* 2.44(1.45~3.44)* lag2 0.73(0.16~1.31)* 0.55(0.09~1.01)* 3.53(1.48~5.62)* 2.43(1.44~3.42)* lag3 1.17(0.61~1.73)* 1.05(0.61~1.50)* 4.54(2.51~6.60)* 2.18(1.20~3.17)* lag4 1.20(0.64~1.76)* 1.02(0.57~1.47)* 4.20(2.18~6.26)* 1.84(0.86~2.83)* lag5 0.86(0.29~1.42)* 0.66(0.21~1.12)* 2.92(0.89~4.99)* 1.45(0.46~2.44)* lag01 1.26(0.61~1.92)* 1.03(0.50~1.57)* 2.69(0.33~5.11)* 2.18(1.07~3.29)* lag02 1.46(0.72~2.19)* 1.17(0.57~1.77)* 3.72(1.23~6.28)* 2.93(1.72~4.15)* lag03 1.87(1.08~2.68)* 1.56(0.92~2.22)* 4.84(2.25~7.50)* 3.45(2.15~4.76)* lag04 2.26(1.41~3.12)* 1.89(1.20~2.58)* 5.55(2.87~8.30)* 3.77(2.40~5.16)* lag05 2.47(1.56~3.38)* 2.02(1.29~2.75)* 5.75(2.99~8.58)* 3.93(2.49~5.39)* [注] *: P< 0.05。 累积滞后结果显示,PM2.5、PM10、SO2、NO2在lag01~lag05均有统计学意义(P<0.05)。PM2.5、PM10、SO2、NO2的累积滞后效应均在lag05最大,其对应的ER及其95%CI分别为2.47% (1.56%~3.38%)、2.02%(1.29%~2.75%)、5.75%(2.99%~8.58%)和3.93%(2.49%~5.39%)(表3)。
2.4 双污染物模型结果
选择Spearman相关系数小于0.7的污染物纳入双污染物模型,结果显示,各污染物调整前后结果均有统计学意义(P<0.05),双污染物模型结果与单污染物模型结果效应值差异无统计学意义(P>0.05)。双污染物模型结果与单污染物模型结果基本一致,且95%CI变化范围也较小(表4)。
表 4 2013—2019年上海市静安区大气污染对糖尿病相关疾病死亡风险的双污染物模型Table 4. Double-pollutant model of diabetes related mortality in association with air pollutants in Shanghai Jing'an District from 2013 to 2019污染物 最佳滞后日 调整因素 ER(95%CI)/% PM2.5 lag05 — 2.47(1.56~3.38)* SO2 2.77(1.78~3.77)* NO2 2.49(1.50~3.48)* PM10 lag05 — 2.02(1.29~2.75)* SO2 2.34(1.53~3.16)* NO2 2.03(1.24~2.82)* SO2 lag05 — 5.75(2.99~8.58)* PM2.5 4.19(2.14~6.27)* PM10 4.16(2.10~6.25)* NO2 4.27(2.19~6.39)* NO2 lag05 — 3.93(2.49~5.39)* PM2.5 3.85(2.25~5.48)* PM10 3.84(2.25~5.46)* SO2 4.51(2.92~6.13)* [注] *:P< 0.05。 2.5 大气污染物对不同性别、年龄人群糖尿病相关疾病死亡的影响
分层分析结果显示,lag05时PM2.5、PM10、SO2、NO2浓度增加对男性、女性和≥65岁人群糖尿病相关疾病死亡风险升高均有统计学意义(P<0.05),对<65岁人群糖尿病相关疾病死亡效应无统计学意义。但性别、年龄组间的效应值差异均无统计学意义(P>0.05)(表5)。
表 5 2013—2019年上海市静安区大气污染物对不同性别、年龄人群糖尿病相关疾病死亡的超额危险度[ER(95%CI)/%]Table 5. Excess risk of diabetes related mortality stratified by gender and age groups in Shanghai Jing'an District from 2013 to 2019 [ER(95%CI)/%]指标 PM2.5 PM10 SO2 NO2 男性 2.03(0.73~3.34)* 1.79(0.75~2.84)* 6.31(2.38~10.39)* 3.62(1.59~5.69)* 女性 2.89(1.63~4.16)* 2.24(1.22~3.26)* 5.24(1.42~9.21)* 4.23(2.21~6.30)* <65岁 2.50(-0.19~5.26) 2.11(-0.07~4.33) 1.32(-6.66~9.98) 2.76(-1.52~7.22) ≥65岁 2.46(1.51~3.43)* 2.01(1.24~2.78)* 6.30(3.38~9.31)* 4.07(2.55~5.62)* [注] *:P< 0.05。 2.6 暴露-反应关系曲线
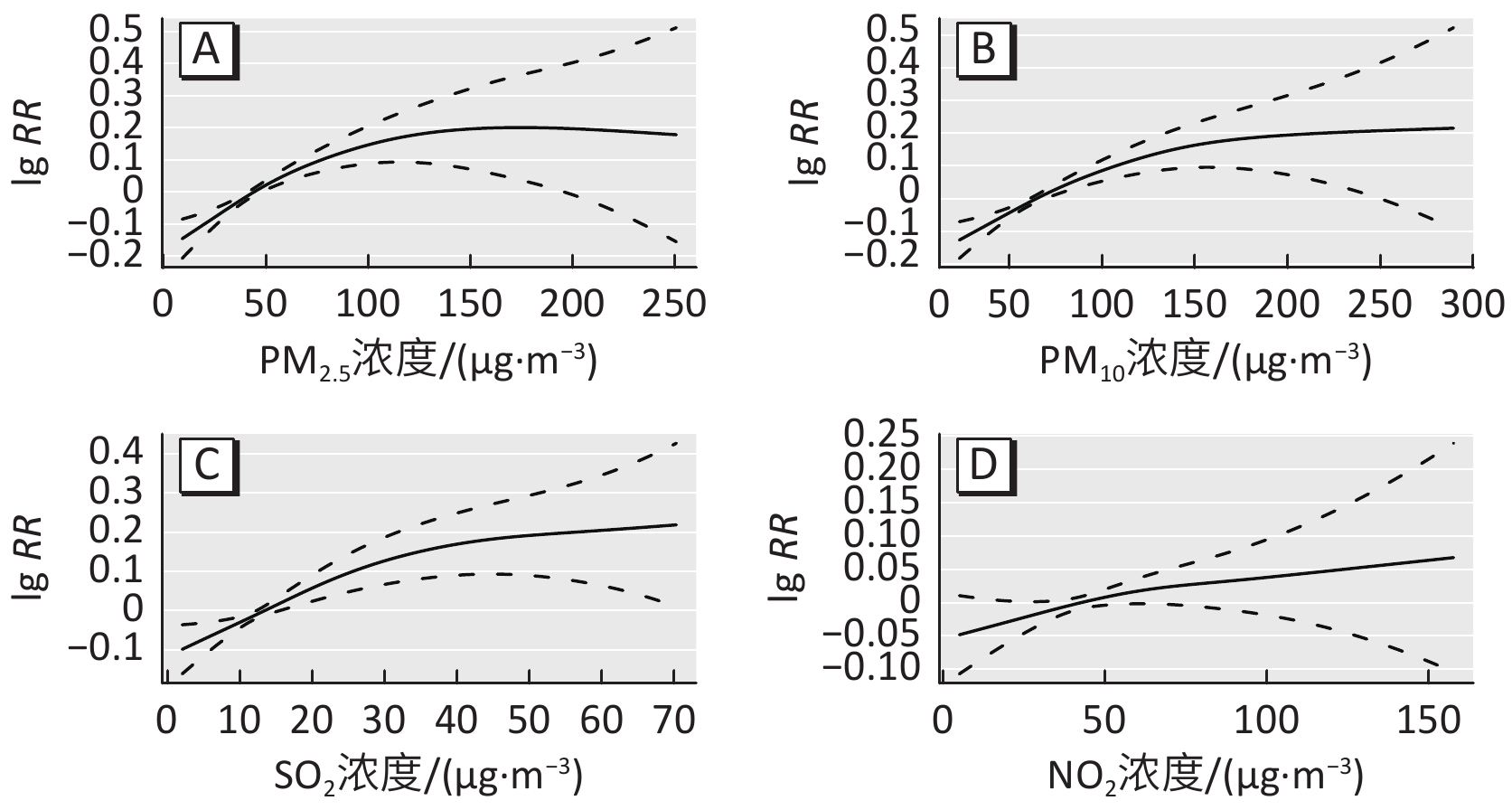
PM2.5、PM10、SO2、NO2浓度(lag05)与糖尿病死亡风险的暴露-反应关系曲线均呈近似线性递增,但斜率稍有差异。在高浓度下,暴露-反应曲线趋向平坦(图1)。
3. 讨论
本研究结果显示,2013—2019年上海市静安区大气污染物SO2和NO2达到国家环境空气质量一级标准,PM2.5和PM10达到国家环境空气质量二级标准。近年来国家和政府加强了对空气污染的治理,静安区也重点开展了锅炉提标改造、挥发性有机物源头减排、餐饮油烟在线监控和第三方治理、区域扬尘监管等工作[20],环境质量明显改善,但大气污染物浓度仍高于世界卫生组织《空气质量指南》中的准则值[21],大气污染问题仍较为突出,提示今后需继续加强大气污染物的监测与控制。
本研究结果显示,短期暴露于大气污染物会增加居民糖尿病相关疾病死亡风险,且存在滞后效应,在lag05时效应最大,PM2.5、PM10、SO2、NO2质量浓度每增加10μg·m−3,死亡风险分别增加2.47%(95%CI: 1.56%~3.38%)、2.02%(95%CI: 1.29%~2.75%)、5.75%(95%CI: 2.99%~8.58%)和3.93%(95%CI: 2.49%~5.39%)。加拿大的研究发现,PM2.5浓度每增加一个四分位数间距,糖尿病相关疾病死亡风险增加3.69%(95%CI: 0.67%~6.80%)[22]。意大利的一项研究发现PM2.5、PM10、NO2会增加糖尿病相关疾病的死亡风险,其浓度每增加10 μg·m−3,相应的死亡风险增加1.98%(95%CI:0.54%~3.44%)[9]、1.03%(95%CI:0.28%~1.79%)[23]、3.61%(95%CI:1.73%~5.53%)[24]。本研究结果与国外研究结果存在差异,可能原因为不同地区大气污染物浓度、污染物来源及成分、人群易感性等因素存在差异。
本研究结果显示,SO2和NO2的对糖尿病相关疾病死亡的效应值高于大气颗粒物的效应值。参考既往研究,可以发现SO2、NO2等气态污染物对我国居民死亡的影响一直高于颗粒物[25-27],且SO2的效应值高于NO2[28],可能原因为SO2浓度与死亡率的暴露-反应关系在低浓度下更强[29],在低浓度下仍对死亡有影响[30]。同时,本研究发现PM2.5对糖尿病相关疾病死亡的效应值高于PM10,与其他研究结果一致[31]。但也有美国和中国的队列研究结果显示[32-33],大气颗粒物对糖尿病死亡风险的长期影响高于SO2、NO2等气态污染物。今后可收集长期资料,通过队列研究确认大气污染对居民糖尿病相关疾病死亡的长期影响。
双污染物模型中,分别调整其他污染物后的结果与单污染物模型结果基本保持一致,提示单污染物模型稳健性良好。但双污染物模型结果与单污染物模型结果效应值差异无统计学意义。与既往研究结果有所不同,上海先前的研究发现,在调整其他污染物后,PM10、SO2、NO2对糖尿病死亡的相对危险度均下降[34];欧洲的研究在调整了其他污染物之后,发现PM2.5对糖尿病死亡的影响减小[35]。上述研究结果差异提示由于大气污染的浓度特征不同,污染物之间的相互作用也存在一定差异。
为了探寻大气污染对糖尿病死亡的易感人群,本研究对不同性别、年龄的人群进行了分层分析。结果显示不同性别间的差异尚未达到有统计学意义的程度。南京的研究发现PM10、SO2、NO2浓度增高对男性糖尿病死亡风险的影响大于女性[36]。加拿大一项研究则发现,PM2.5暴露对男性糖尿病死亡风险高于女性[7]。本研究结果与之前有关性别差异的研究并不一致,可能原因为静安区糖尿病相关疾病粗死亡率性别差异不大,仅在部分年份存在差异[37],且不同性别吸烟饮酒等行为危险因素存在差异,本研究未识别并校正混杂因素的影响。
本研究发现大气污染物会增加≥65岁人群糖尿病相关疾病死亡的风险,<65岁人群糖尿病相关疾病死亡效应无统计学意义。此前的一些研究已经确认了老年人短期暴露于PM2.5、PM10和SO2等大气污染物时,会增加该人群糖尿病死亡风险[9, 38]。可能是高龄人群有较高的患病率,且呼吸道和心血管对污染物的清除能力较差,暴露于PM2.5后容易加重病情而导致死亡[39]。因此高龄人群对大气污染物的易感性较高。
本研究的不足之处:首先, 本研究的大气污染数据来源于固定的室外空气监测点,而大部分人不仅受室外空气污染的影响,还受到吸烟、烹饪、装修材料污染等室内污染因素的影响[40]。因此,通过室外大气污染的浓度来评估实际的暴露程度可能存在偏倚。其次,糖尿病患者可能同时患有多种慢性病和并发症[41],医生最终填写死亡证时可能漏报告糖尿病[42],采用死亡证明中所有提及糖尿病死亡的数据可能仍低估糖尿病相关疾病死亡的实际负担。且糖尿病患者的主要死亡原因为心脑血管疾病[43],糖尿病患者是否更多地受到大气污染对循环系统疾病的影响有待研究。此外,本研究未区分大气污染对1型或2型糖尿病的死亡效应。
综上所述,上海市静安区大气污染物PM2.5、PM10、SO2、NO2短期暴露会导致人群糖尿病相关疾病死亡风险增加,且这种风险存在滞后效应和累积效应,≥65岁人群是受大气污染对糖尿病相关疾病死亡影响的易感人群。
-
表 1 2013—2019年上海市静安区糖尿病相关疾病死亡、大气污染物浓度水平及气象因素的分布
Table 1 Daily diabetes related deaths, concentrations of air pollutants, and levels of meteorological factors in Shanghai Jing'an District from 2013 to 2019
指标 ${\bar x}$±s Min P25 P50 P75 Max 死亡指标 糖尿病相关疾病死亡人数 4.27±2.22 0.00 3.00 4.00 6.00 16.00 男性 2.11±1.50 0.00 1.00 2.00 3.00 11.00 女性 2.15±1.52 0.00 1.00 2.00 3.00 9.00 <65岁 0.47±0.69 0.00 0.00 0.00 1.00 4.00 ≥65岁 3.80±2.08 0.00 2.00 4.00 5.00 15.00 大气污染物浓度/(μg·m−3) PM10 68.12±42.60 7.00 40.20 57.17 82.54 561.32 PM2.5 47.16±34.23 4.67 23.63 38.38 59.55 505.78 SO2 14.09±10.96 1.74 7.50 11.04 16.84 105.70 NO2 46.29±21.67 5.08 30.57 42.17 57.64 157.63 气象指标 温度/℃ 17.48±8.72 −6.10 9.80 18.40 24.40 35.00 相对湿度/% 72.71±12.55 27.50 64.30 74.00 82.00 99.30 表 2 2013—2019年上海市静安区大气污染物与气象因素相关性分析(r)
Table 2 Correlation analysis between air pollutants and meteorological factors in Shanghai Jing'an District from 2013 to 2019 (r)
指标 PM2.5 SO2 NO2 温度 相对湿度 PM10 0.88* 0.62* 0.64* −0.22* −0.32* PM2.5 1.00 0.61* 0.68* −0.27* −0.13* SO2 1.00 0.61* −0.45* −0.41* NO2 1.00 −0.51* −0.10* 温度 1.00 0.12* [注] *:P< 0.05。 表 3 2013—2019年上海市静安区大气污染物对糖尿病相关疾病死亡的超额危险度[ER(95%CI)/%]
Table 3 Excess risk of diabetes related mortality in association with air pollutants in Shanghai Jing'an District from 2013 to 2019 [ER(95%CI)/%]
滞后天数 PM2.5 PM10 SO2 NO2 lag0 0.78(0.22~1.35)* 0.63(0.17~1.10)* 0.89(−1.26~3.08) 1.04(0.06~2.04)* lag1 1.11(0.55~1.68)* 0.90(0.44~1.36)* 3.32(1.23~5.47)* 2.44(1.45~3.44)* lag2 0.73(0.16~1.31)* 0.55(0.09~1.01)* 3.53(1.48~5.62)* 2.43(1.44~3.42)* lag3 1.17(0.61~1.73)* 1.05(0.61~1.50)* 4.54(2.51~6.60)* 2.18(1.20~3.17)* lag4 1.20(0.64~1.76)* 1.02(0.57~1.47)* 4.20(2.18~6.26)* 1.84(0.86~2.83)* lag5 0.86(0.29~1.42)* 0.66(0.21~1.12)* 2.92(0.89~4.99)* 1.45(0.46~2.44)* lag01 1.26(0.61~1.92)* 1.03(0.50~1.57)* 2.69(0.33~5.11)* 2.18(1.07~3.29)* lag02 1.46(0.72~2.19)* 1.17(0.57~1.77)* 3.72(1.23~6.28)* 2.93(1.72~4.15)* lag03 1.87(1.08~2.68)* 1.56(0.92~2.22)* 4.84(2.25~7.50)* 3.45(2.15~4.76)* lag04 2.26(1.41~3.12)* 1.89(1.20~2.58)* 5.55(2.87~8.30)* 3.77(2.40~5.16)* lag05 2.47(1.56~3.38)* 2.02(1.29~2.75)* 5.75(2.99~8.58)* 3.93(2.49~5.39)* [注] *: P< 0.05。 表 4 2013—2019年上海市静安区大气污染对糖尿病相关疾病死亡风险的双污染物模型
Table 4 Double-pollutant model of diabetes related mortality in association with air pollutants in Shanghai Jing'an District from 2013 to 2019
污染物 最佳滞后日 调整因素 ER(95%CI)/% PM2.5 lag05 — 2.47(1.56~3.38)* SO2 2.77(1.78~3.77)* NO2 2.49(1.50~3.48)* PM10 lag05 — 2.02(1.29~2.75)* SO2 2.34(1.53~3.16)* NO2 2.03(1.24~2.82)* SO2 lag05 — 5.75(2.99~8.58)* PM2.5 4.19(2.14~6.27)* PM10 4.16(2.10~6.25)* NO2 4.27(2.19~6.39)* NO2 lag05 — 3.93(2.49~5.39)* PM2.5 3.85(2.25~5.48)* PM10 3.84(2.25~5.46)* SO2 4.51(2.92~6.13)* [注] *:P< 0.05。 表 5 2013—2019年上海市静安区大气污染物对不同性别、年龄人群糖尿病相关疾病死亡的超额危险度[ER(95%CI)/%]
Table 5 Excess risk of diabetes related mortality stratified by gender and age groups in Shanghai Jing'an District from 2013 to 2019 [ER(95%CI)/%]
指标 PM2.5 PM10 SO2 NO2 男性 2.03(0.73~3.34)* 1.79(0.75~2.84)* 6.31(2.38~10.39)* 3.62(1.59~5.69)* 女性 2.89(1.63~4.16)* 2.24(1.22~3.26)* 5.24(1.42~9.21)* 4.23(2.21~6.30)* <65岁 2.50(-0.19~5.26) 2.11(-0.07~4.33) 1.32(-6.66~9.98) 2.76(-1.52~7.22) ≥65岁 2.46(1.51~3.43)* 2.01(1.24~2.78)* 6.30(3.38~9.31)* 4.07(2.55~5.62)* [注] *:P< 0.05。 -
[1] GBD 2017 Causes of Death Collaborators. Global, regional, and national age-sex-specific mortality for 282 causes of death in 195 countries and territories, 1980-2017: a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2018, 392(10159): 1736-1788. doi: 10.1016/S0140-6736(18)32203-7
[2] International Diabetes Federation. IDF Diabetes atlas 9th edition 2019[EB/OL]. [2020-11-30]. https://diabetesatlas.org/en/.
[3] 上海市统计局. 2019年上海统计年鉴[EB/OL]. [2020-10-06]. http://tjj.sh.gov.cn/tjnj/20200427/4aa08fba106d45fda6cb39817d961c98.html. Shanghai Municipal Bureau of Statistics. Shanghai statistical yearbook 2019[EB/OL]. [2020-10-06]. http://tjj.sh.gov.cn/tjnj/20200427/4aa08fba106d45fda6cb39817d961c98.html.
[4] American Diabetes Association. Classification and diagnosis of diabetes: standards of medical care in diabetes-2019[J]. Diabetes Care, 2019, 42(S1): S13-S28.
[5] RAO X, PATEL P, PUETT R, et al. Air pollution as a risk factor for type 2 diabetes[J]. Toxicol Sci, 2015, 143(2): 231-241. doi: 10.1093/toxsci/kfu250
[6] GBD 2017 Risk Factor Collaborators. Global, regional, and national comparative risk assessment of 84 behavioural, environmental and occupational, and metabolic risks or clusters of risks for 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2018, 392(10159): 1923-1994. doi: 10.1016/S0140-6736(18)32225-6
[7] Brook RD, Cakmak S, Turner MC, et al. Long-term fine particulate matter exposure and mortality from diabetes in Canada[J]. Diabetes Care, 2013, 36(10): 3313-3320. doi: 10.2337/dc12-2189
[8] OSTRO B, BROADWIN R, GREEN S, et al. Fine particulate air pollution and mortality in nine California counties: results from CALFINE[J]. Environ Health Perspect, 2006, 114(1): 29-33. doi: 10.1289/ehp.8335
[9] ALESSANDRINI E R, STAFOGGIA M, FAUSTINI A, et al. Association between short-term exposure to PM2.5 and PM10 and mortality in susceptible subgroups: a multisite case-crossover analysis of individual effect modifiers[J]. Am J Epidemiol, 2016, 184(10): 744-754. doi: 10.1093/aje/kww078
[10] DUBOWSKY S D, SUH H, SCHWARTZ J, et al. Diabetes, obesity, and hypertension may enhance associations between air pollution and markers of systemic inflammation[J]. Environ Health Perspect, 2006, 114(7): 992-998. doi: 10.1289/ehp.8469
[11] HAN Y, WANG Y, LI W, et al. Susceptibility of prediabetes to the health effect of air pollution: a community-based panel study with a nested case-control design[J]. Environ Health, 2019, 18(1): 65. doi: 10.1186/s12940-019-0502-6
[12] PARK S K, O'NEILL M S, VOKONAS P S, et al. Effects of air pollution on heart rate variability: the VA normative aging study[J]. Environ Health Perspect, 2005, 113(3): 304-309. doi: 10.1289/ehp.7447
[13] LIU C, YANG C, ZHAO Y, et al. Associations between long-term exposure to ambient particulate air pollution and type 2 diabetes prevalence, blood glucose and glycosylated hemoglobin levels in China[J]. Environ Int, 2016, 92-93: 416-421. doi: 10.1016/j.envint.2016.03.028
[14] CHUANG K J, YAN Y H, CHENG T J. Effect of air pollution on blood pressure, blood lipids, and blood sugar: a population-based approach[J]. J Occup Environ Med, 2010, 52(3): 258-262. doi: 10.1097/JOM.0b013e3181ceff7a
[15] SUN Q, YUE P, DEIULIIS J A, et al. Ambient air pollution exaggerates adipose inflammation and insulin resistance in a mouse model of diet-induced obesity[J]. Circulation, 2009, 119(4): 538-546. doi: 10.1161/CIRCULATIONAHA.108.799015
[16] BRACCO P A, GREGG E W, ROLKA D B, et al. A nationwide analysis of the excess death attributable to diabetes in Brazil[J]. J Glob Health, 2020, 10(1): 010401. doi: 10.7189/jogh.10.010401
[17] JOUGLA E, PAPOZ L, BALKAU B, et al. Death certificate coding practices related to diabetes in European countries—the 'EURODIAB subarea C' study[J]. Int J Epidemiol, 1992, 21(2): 343-351. doi: 10.1093/ije/21.2.343
[18] RAO C, ADAIR T, BAIN C, et al. Mortality from diabetic renal disease: a hidden epidemic[J]. Eur Public Health, 2012, 22(2): 280-284. doi: 10.1093/eurpub/ckq205
[19] LU T H, KWOK C F, HO L T. Whether to report diabetes as the underlying cause-of-death? a survey of internists of different sub-specialties[J]. BMC Endocr Disord, 2010, 10: 13. doi: 10.1186/1472-6823-10-13
[20] 上海市静安区生态环境局. 2019静安区生态环境公报[EB/OL]. (2020-06-11) [2020-12-01]. https://www.jingan.gov.cn/govxxgk/JC4/2020-06-11/0be09be4-eb9c-4b1c-bb13-d4821b6ca7e9.html. Shanghai Jing'an District Ecological Environment Bureau. Ecological environment bulletin of Jing'an District 2019[EB/OL]. (2020-06-06)[2020-12-01]. https://www.jingan.gov.cn/govxxgk/JC4/2020-06-11/0be09be4-eb9c-4b1c-bb13-d4821b6ca7e9.html.
[21] World Health Organization. Air quality guidelines global update 2005[M]. Geneva: World Health Organization, 2006.
[22] GOLDBERG M S, BURNETT R T, YALE J F, et al. Associations between ambient air pollution and daily mortality among persons with diabetes and cardiovascular disease[J]. Environ Res, 2006, 100(2): 255-267. doi: 10.1016/j.envres.2005.04.007
[23] FORASTIERE F, STAFOGGIA M, BERTI G, et al. Particulate matter and daily mortality: a case-crossover analysis of individual effect modifiers[J]. Epidemiology, 2008, 19(4): 571-580. doi: 10.1097/EDE.0b013e3181761f8a
[24] CHIUSOLO M, CADUM E, STAFOGGIA M, et al. Short-term effects of nitrogen dioxide on mortality and susceptibility factors in 10 Italian cities: the EpiAir study[J]. Environ Health Perspect, 2011, 119(9): 1233-1238. doi: 10.1289/ehp.1002904
[25] 阚海东, 陈秉衡, 贾健. 上海市大气污染与居民每日死亡关系的病例交叉研究[J]. 中华流行病学杂志, 2003, 24(10): 863-867. doi: 10.3760/j.issn:0254-6450.2003.10.003 KAN H D, CHEN B H, JIA J. A case-crossover study of ambient air pollution and daily mortality in Shanghai[J]. Chin J Epidemiol, 2003, 24(10): 863-867. doi: 10.3760/j.issn:0254-6450.2003.10.003
[26] 钱轶峰, 韩明, 靳文正, 等. 上海市大气污染与慢性阻塞性肺病死亡的关联性[J]. 环境与职业医学, 2015, 32(12): 1093-1097. QIAN Y F, HAN M, JIN W Z, et al. Association between ambient air pollution and COPD mortality in Shanghai[J]. J Environ Occup Med, 2015, 32(12): 1093-1097.
[27] SHANG Y, SUN Z, CAO J, et al. Systematic review of Chinese studies of short-term exposure to air pollution and daily mortality[J]. Environ Int, 2013, 54: 100-111. doi: 10.1016/j.envint.2013.01.010
[28] HE T, YANG Z, LIU T, et al. Ambient air pollution and years of life lost in Ningbo, China[J]. Sci Rep, 2016, 6: 22485. doi: 10.1038/srep22485
[29] SAMOLI E, SCHWARTZ J, WOJTYNIAK B, et al. Investigating regional differences in short-term effects of air pollution on daily mortality in the APHEA project: a sensitivity analysis for controlling long-term trends and seasonality[J]. Environ Health Perspect, 2001, 109(4): 349-353. doi: 10.1289/ehp.01109349
[30] WONG C M, MA S, HEDLEY A J, et al. Effect of air pollution on daily mortality in Hong Kong[J]. Environ Health Perspect, 2001, 109(4): 335-340. doi: 10.1289/ehp.01109335
[31] LI C, FANG D, XU D, et al. MECHANISMS IN ENDOCRINOLOGY: main air pollutants and diabetes-associated mortality: a systematic review and meta-analysis[J]. Eur J Endocrinol, 2014, 171(5): R183-R190. doi: 10.1530/EJE-14-0287
[32] LIM C C, HAYES R B, AHN J, et al. Association between long-term exposure to ambient air pollution and diabetes mortality in the US[J]. Environ Res, 2018, 165: 330-336. doi: 10.1016/j.envres.2018.04.011
[33] SHAN A, ZHANG Y, ZHANG L W, et al. Associations between the incidence and mortality rates of type 2 diabetes mellitus and long-term exposure to ambient air pollution: a 12-year cohort study in northern China[J]. Environ Res, 2020, 186: 109551. doi: 10.1016/j.envres.2020.109551
[34] 阚海东, 贾健, 陈秉衡. 上海市某区大气污染与居民糖尿病死亡关系的时间序列研究[J]. 上海环境科学, 2003, 22(12): 955-957,966. KAN H D, JIA J, CHEN B H. A time-series study on association of ambient air pollution and diabetes mortality in Shanghai[J]. Shanghai Environ Sci, 2003, 22(12): 955-957,966.
[35] SAMOLI E, STAFOGGIA M, RODOPOULOU S, et al. Which specific causes of death are associated with short term exposure to fine and coarse particles in Southern Europe? Results from the MED-PARTICLES project[J]. Environ Int, 2014, 67: 54-61. doi: 10.1016/j.envint.2014.02.013
[36] 张瑞明, 李润奎, 罗凯, 等. 空气中SO2和NO2对糖尿病患者影响的病例交叉研究[J]. 基础医学与临床, 2017, 37(6): 812-816. doi: 10.3969/j.issn.1001-6325.2017.06.014 ZHANG R M, LI R K, LUO K, et al. Association of the exposure of SO2 and NO2 with diabetes: a case-crossover study[J]. Basic Clin Med, 2017, 37(6): 812-816. doi: 10.3969/j.issn.1001-6325.2017.06.014
[37] 褚晓婷, 熊建菁, 张国慧, 等. 2005—2019年上海市静安区居民糖尿病相关疾病死亡变化趋势分析[J]. 中国慢性病预防与控制, 2021, 29(5): 397-401. CHU X T, XIONG J J, ZHANG G H, et al. Trend of diabetes mellitus related mortality in Shanghai Jing’an District, 2005-2019[J]. Chin J Prev Contr Chron Dis, 2021, 29(5): 397-401.
[38] BATESON T F, SCHWARTZ J. Who is sensitive to the effects of particulate air pollution on mortality? A case-crossover analysis of effect modifiers[J]. Epidemiology, 2004, 15(2): 143-149. doi: 10.1097/01.ede.0000112210.68754.fa
[39] BELL M L, ZANOBETTI A, DOMINICI F. Evidence on vulnerability and susceptibility to health risks associated with short-term exposure to particulate matter: a systematic review and meta-analysis[J]. Am J Epidemiol, 2013, 178(6): 865-876. doi: 10.1093/aje/kwt090
[40] 钱华, 戴海夏. 室内空气污染与人体健康的关系[J]. 环境与职业医学, 2007, 24(4): 426-430. QIAN H, DAI H X. Indoor air pollution and its adverse health effects[J]. J Environ Occup Med, 2007, 24(4): 426-430.
[41] MORRISH N J, WANG S L, STEVENS L K, et al. Mortality and causes of death in the WHO Multinational Study of Vascular Disease in Diabetes[J]. Diabetologia, 2001, 44Suppl2: S14-S21.
[42] MCEWEN L N, KARTER A J, CURB J D, et al. Temporal trends in recording of diabetes on death certificates: results from translating research into action for diabetes (TRIAD)[J]. Diabetes Care, 2011, 34(7): 1529-1533. doi: 10.2337/dc10-2312
[43] EINARSON T R, ACS A, LUDWIG C, et al. Prevalence of cardiovascular disease in type 2 diabetes: a systematic literature review of scientific evidence from across the world in 2007-2017[J]. Cardiovasc Diabetol, 2018, 17(1): 83. doi: 10.1186/s12933-018-0728-6
-
期刊类型引用(2)
1. 薛咏茜,胡耀余,章萌,朱倩,胡美玲,李舒婷,谢文涵,李元,欧阳逸馨,刘相佟. 2014—2019年北京市大气NO_2对呼吸系统疾病入院人次的影响. 环境卫生学杂志. 2024(10): 843-849+859 .  百度学术
百度学术
2. 张钰棋,张瑛,曹运长,王五香,封少龙. PM_(2.5)影响2型糖尿病分子机制的研究进展. 生命的化学. 2023(12): 1847-1853 .  百度学术
百度学术
其他类型引用(1)






 下载:
下载: